Бактериофаги (вирусы бактерий)
Строение бактериофагов изучают с помощью электронной микроскопии образцов, контрастированных напылением металлов или фосфорно-вольфрамовой кислотой.
В зависимости от формы и структурной организации фаги подразделяют на несколько морфологических типов :
нитевидные;
мелкие кубические (некоторые из них имеют аналоги отростков), без отростка, с коротким отростком, с длинным отростком;
фаги сперматозоидной формы, т. е. с кубической головкой и хвостовым отростком, имеющие сокращающийся или не сокращающийся чехол отростка.
Размеры фагов колеблются от 20 до 800 нм (нитевидный тип).
Наиболее изучены крупные бактериофаги, имеющие форму сперматозоида и сокращающийся чехол отростка, например, колифаги Т2, Т4, Т6. Они состоят из головки икосаэд рического типа размером 65-100 нм и хвосто вого отростка длиной более 100 нм (рис. 3.14).
Хвостовой отросток имеет внутри полый ци линдрический стержень , сообщающийся с головкой, а снаружи - чехол , способный к сокращению, наподобие мышцы. Чехол присоединен к воротничку, окружающему стержень около головки. На дистальном конце отростка имеется шестиугольная базальная ,пластинка с шипами , от которых отходят нитевидные структуры - фибриллы.
Бактериофаги содержат или ДНК, или РНК. Нуклеиновые кислоты фагов могут быть двунитевыми, однонитевыми, линейными, кольцевыми. Большинство фагов содержит двунитевую ДНК, замкнутую в кольцо.
У фагов, имеющих форму сперматозоида, одна молекула двунитевой суперспирализованной ДНК находится внутри головки и защищена капсидом. Капсид состоит из белковых молекул - идентичных полипептидных субъединиц, уложенных по икосаэдрическому (кубическому) типу симметрии. В состав головки также входит полипептид, состоящий из аспарагиновой, глутаминовой кислот и лизина. У некоторых фагов внутри головки находится внутренний гистоноподобный белок, обеспечивающий суперспирализацию ДНК. Сокращающийся чехол хвостового отростка образован также белковыми субъединицами, уложенными по спиральному типу симметрии, содержащими АТФ и ионы Са 2+ . У некоторых фагов (например, Т2) в дистальной части отростка содержится фермент лизоцим.
Антигенные свойства. Бактериофаги содержат группоспецифические и типоспецифические антигены, обладают иммуногенными свойствами, вызывая синтез специфических антител в организме. Антитела, взаимодействуя с бактериофагами, могут нейтрализовать их литическую активность против бактерий. По типоспецифическим антигенам фаги делят на серотипы.
Резистентность. По сравнению с вирусами человека бактериофаги более устойчивы к факторам окружающей среды. Инактивируются под действием температуры 65-70 °С, УФ-облучения в высоких дозах, ионизирующей радиации, формалина и кислот. Длительно сохраняются при низкой температуре и высушивании.
Взаимодействие фагов с бактериальной клеткой. Бактериофаги инфицируют строго определенные бактерии, взаимодействуя со специфическими рецепторами клетки.
По специфичности взаимодействия различают следующие бактериофаги:
поливалентные, взаимодействующие с родственными видами бактерий;
моновалентные, взаимодействующие с бактериями определенного вида;
типовые, взаимодействующие с отдельными типами (вариантами) бактерий данного вида.
Взаимодействие фагов с бактериями может протекать, как и у других вирусов, по:
продуктивному,
абортивному
интегративному типам.
При продуктивном типе взаимодействия образуется фаговое потомство, бактерии лизируются; при абортивном типе - фаговое потомство не образуется и бактерии сохраняют свою жизнедеятельность; при интегративном типе - геном фага встраивается в хромосому бактерии и сосуществует с ней.
В зависимости от типа взаимодействия различают вирулент ные и умеренные бактериофаги.
Вирулентные бактериофаги взаимодействуют с бактерией по продуктивному типу. Проникнув в бактерию, они репродуцируются с образованием 200-300 новых фаговых частиц и вызывают лизис бактерий. Взаимодействие бактериофага с бактерией напоминает взаимодействие вирусов человека с клеткой хозяина. Специфическая адсорбция фагов на бактериальной клетке происходит при наличии комплементарных рецепторов липопротеиновой или липополисахаридной природы в ее клеточной стенке. На бактериях, лишенных клеточной стенки (протопласты, сферопласты), бактериофаги не адсорбируются. Некоторые фаги в качестве рецепторов используют половые пили бактерий.
Фаги, имеющие хвостовой отросток, прикрепляются к бактериальной клетке свободным концом отростка (фибриллами, базальной пластинкой). Проникновение фаговой нуклеиновой кислоты в бактерию наиболее изучено у бактериофагов, имеющих отросток с сокращающимся чехлом. В результате активации АТФ чехол хвостового отростка сокращается, и стержень с помощью лизоцима, растворяющего прилегающий фрагмент клеточной стенки, как бы просверливает оболочку клетки. При этом ДНК фага, содержащаяся в его головке, проходит в форме нити через канал хвостового стержня и инъецируется в клетку, а капсид фага остается снаружи бактерии.
Некоторые мелкие кубические фаги, способные адсорбироваться на половых пилях, вводят свою нуклеиновую кислоту через канал этих пилей. ДНК нитевидных фагов проходит в бактерию вместе с одним из капсид-ных белков.
Инъецированная внутрь бактерии нуклеиновая кислота подавляет биосинтез компонентов клетки, заставляя ее синтезировать нуклеиновую кислоту и белки фага. Эти процессы схожи с репродукцией вирусов человека. После образования компонентов фага происходит самосборка частиц: сначала пустотелые капсиды головок заполняются нуклеиновой кислотой, затем сформированные головки соединяются с хвостовыми отростками. В результате изменения внутриклеточного осмотического давления и действия фагового лизоцима происходит разрушение оболочки, лизис бактерии и выход фагов из нее. Весь литический цикл от адсорбции бактериофага на бактерии до его выхода из нее занимает 20-40 мин.
Умеренные бактериофаги в отличие от вирулентных взаимодействуют с чувствительными бактериями либо по продуктивному, либо по интегративному типу. Продуктивный цикл умеренного фага идет в той же последовательности, что и у вирулентных фагов, и заканчивается лизисом клетки. При интегративном типе взаимодействия ДНК умеренного фага встраивается в хромосому бактерии, реплицируется синхронно с геномом размножающейся бактерии, не вызывая ее лизиса. ДНК бактериофага, встроенная в хромосому бактерии, называется профагом, а культура бактерий - лизогенной. Такое сосуществование бактерии и умеренного бактериофага называется лизогенией (от греч. lysis - разложение, genea - происхождение). Профаг, ставший частью хромосомы бактерии, при ее размножении передается по наследству потомкам.
Каким образом нуклеиновая кислота присоединяется к бактериальной хромосоме?После проникновения в бактерию ДНК умеренного фага приобретает форму кольца, а затем интегрирует по типу кроссинговера в строго определенную гомологичную область хромосомы клетки.
Итак, при лизогении образование фагового потомства не происходит. В основе «сдерживающего» механизма репродукции фагов лежит образование в бактерии специфического репрессора - низкомолекулярного белка, подавляющего транскрипцию фаговых генов. Биосинтез репрессора детерминируется генами профага. Наличием репрессора можно объяснить способность лизогенных бактерий приобретать иммунитет (невосприимчивость) к последующему заражению гомологичным или близкородственными фагами. Под иммунитетом в данном случае понимается такое состояние бактерии, при котором исключается процесс вегетативного размножения вышеуказанных фагов и лизис клетки. Однако термин «лизогения» отражает потенциальную возможность лизиса бактерии, содержащей профаг. Действительно, профаги некоторой части лизогенной культуры бактерий могут спонтанно (самопроизвольно) или направленно под действием ряда физических или химических факторов дерепрессироваться, исключаться из хромосомы, переходить в вегетативное состояние. Этот процесс заканчивается продукцией фагов и лизисом бактерий. Частота спонтанного лизиса бактерий в лизогенных культурах невелика (10 2 , 10~ 6), т. е. не захватывает все клетки, обладающие иммунитетом. Частоту лизиса бактерий можно значительно увеличить, воздействуя на лизогенную культуру индуцирующими агентами (УФ-лучи, ионизирующее излучение, перекисные соединения, митомицин С и др.). Сам же феномен воздействия, приводящий к инактивации репрессора, называется индукцией профага. Явление индукции используют в генной инженерии. Однако спонтанный лизис лизогенных культур может нанести вред микробиологическому производству. Так, если микроорганизмы - продуценты биологически активных веществ оказываются лизогенными, существует опасность перехода фага в вегетативное состояние, что приведет к лизису производственного штамма этого микроба.
Геном профага может придавать бактерии новые, ранее отсутствовавшие у нее свойства. Этот феномен изменения свойств микроорганизмов под влиянием профага получил название фаговой конверсии (от лат. conver - sio - превращение). Конвертироваться могут морфологические, культуральные, биохимические, антигенные и другие свойства бактерий. Например, наличие профага в дифтерийной палочке обусловливает ее способность продуцировать дифтерийный экзотоксин.
Умеренные фаги могут быть дефектными, т. е. неспособными образовывать зрелые фаговые частицы ни в естественных условиях, ни при индукции. Геном некоторых умеренных фагов (Р1) может находиться в цитоплазме бактериальной клетки в так называемой плаз-мидной форме, не включаясь в ее хромосому. Такого рода умеренные фаги используют в качестве векторов в генной инженерии.
Практическое применение фагов. Бактериофаги используют в лабораторной диагностике инфекций при внутривидовой идентификации бактерий, т. е. определении фаговара (фаготипа). Для этого применяют метод фаготипирования , основанный на строгой специфичности действия фагов: на чашку с плотной питательной средой, засеянной «газоном» чистой культурой возбудителя, наносят капли различных диагностических типоспецифических фагов. Фаговар бактерии определяется тем типом фага, который вызвал ее лизис (образование стерильного пятна, «бляшки», или «негативной колонии», фага). Методику фаготипирования используют для выявления источника и путей распространения инфекции (эпидемиологическое маркирование). Выделение бактерий одного фаговара от разных больных указывает на общий источник их заражения.
Фаги применяют также для лечения и про филактики ряда бактериальных инфекций. Производят брюшнотифозный, сальмонел-лезный, дизентерийный, синегнойный, стафилококковый, стрептококковый фаги и комбинированные препараты (колипротейный, пиобактериофаги и др). Бактериофаги назначают по показаниям перорально, парентерально или местно в виде жидких, таблетированных форм, свечей или аэрозолей.
Бактериофаги широко применяют в генной инженерии в качестве векторов для получения рекомбинантных ДНК.
Качественный метод определения фагов E . coli . Чашку Петри с питательным агаром засевают суточной бульонной культурой кишечной палочки газоном и подсушивают при 37 "С втечение 10-15 мин. Затем на поверхность газона наносят каплю фага и наклоняют так, чтобы капля стекла к противоположному краю. После суточной инкубации в термостате просматривают чашку, отмечая наличие зоны лизиса по месту стекания капли фага.
Количественный метод - определение титра фага по методу Грациа. Для постановки опыта предварительно: а) разливают питательный агар в чашки Петри, подсушивают в термостате; б) приготовленный полужидкий (0,7 %) питательный агар, разлитый по 3-4 мл в пробирки, растапливают в водяной бане. Делают 10-кратные разведения исследуемого фага (10~ 2 -10~ 7 в зависимости от предполагаемого титра) в изотоническом растворе хлорида натрия. Затем 0,5 мл из последнего разведения фага (10~ 7) смешивают с таким же объемом суточной бульонной культуры чувствительных к фагу бактерий и выливают в пробирку с полужидким агаром, охлажденным до 45 "С. Смесь быстро выливают на поверхность агара в чашке Петри, где она застывает в виде тонкого слоя. Так же готовят смесь из следующего разведения фага (10~ 6) с бактериями и полужидким агаром и выливают на поверхность агара в другой чашке, затем - из разведения 10~ 5 . После застывания второго слоя агара чашки инкубируют при 37 *С, затем подсчитывают число негативных колоний фага. Число этих колоний соответствует количеству фаговых частиц в засеянной смеси. Исходя из него, можно вычислить количество пятнообразующих единиц в 1 мл исходной суспензии фага. Эта величина, характеризующая концентрацию фага, называется его титром (табл. 5.3.1).
Определение спектра литичес кого действия фага. Чашку с питательным агаром делят на квадраты по числу испытуемых бактериальных культур. На каждый квадрат петлей наносят каплю соответствующей бульонной культуры и распределяют ее по агару в пределах данного квадрата. Затем на каждый засеянный квадрат петлей или пастеровской пипеткой наносят по одной капле испытуемого фага. После суточной инкубации в термостате просматривают чашку, отмечая те квадраты, где имеется сплошной лизис бактерий или так называемые стерильные пятна набактериальном газоне. Количество различных бактериальных культур, которые лизируются испытуемым фагом, определяет широту спектра его литического действия.
Фаготипирование бактерий. Испытуемую суточную бульонную культуру бактерий засевают на поверхность питательного агара в чашке Петри, слегка подсушивают в термостате, затем делят на квадраты, на которые пастеровской пипеткой наносят по одной капле различных типоспецифических фагов. После суточной инкубации отмечают на чашке те квадраты, в которых имеется сплошной лизис бактерий. Фаготип бактериальной культуры определяется тем типом фага, который вызывает ее лизис.
Определение лизогении. Исследуемую суточную бульонную культуру центрифугируют для отделения фага от бактерий. В том случае, если бактерии спонтанно продуцируют фаг, последний будет содержаться в надосадочной жидкости. Для выявления фага надосадочную жидкость засевают на газон индикаторной (чувствительной) бактериальной культуры, на котором через
1 сут инкубации при 37 "С образуются очаги лизиса - "стерильные" пятна. При отрицательном результате опыта исследуемую бактериальную культуру предварительно подвергают УФ-облучению с целью индукции содержащегося в ней профага. Затем поступают так же, как и в предыдущем опыте.
Введение............................................................................................3
Морфология Бактериофагов......................................................................3
Физические и Химические Свойства............................................................4
Разнообразие бактериофагов.....................................................................5
Происхождение и природа Бактериофагов....................................................5
Размножение бактериофагов.....................................................................6
Внутриклеточное развитие и явление лизогении..............................................9
Изменчивость и модификации ДНК.............................................................................11
Культивирование бактериофагов................................................................11
Практическое значение фага.......................................................................12
Введение
Бактериофаг, поскольку бактериолитический агент был сначала обнаружен Тортом в 1915, когда он наблюдал любопытное дегенеративное изменение в культурах стафилококков получено из лимфы теленка
Фаги очень использовались в изучении бактериальной генетики и клеточных механизмов управления в значительной степени, потому что бактериальные хозяева так легко вырастают и инфицированы с фагом в лаборатории. Фаги также использовались в попытке уничтожить бактерии, которые причиняют эпидемические болезни, но этот подход был в значительной степени оставлен в 1940-ых, когда антибактериальные лекарства стали доступными. Возможность " фагические терапия " недавно привлекла новый интерес среди медицинских исследователей, однако, вследствие увеличивающейся угрозы, изложенной препарат стойкими бактериями. В 2006 Продовольствие и Администрация Препарата одобрило использование бактериофагов, которые нападают на напряжения лицерия как продовольствие, добавочное на изделиях мяса " готовый есть ".
Морфология и строение бактериофагов
Вирусы, поражающие бактерий, актиномицеты и грибы, называются бактериофагами или просто фагами. Они имеют некоторые особенности необходимо рассмотреть несколько подробнее.
Строение фага более сложно, чем строение вирусов животных и растений. Довольна, своеобразна морфология фага. У него различают головку, имеющую овальную форму
иногда шестигранную, призматическую, иногда круглую. От головки отходит более или менее длинный полый отросток. Фаг сравнивают с барабанной, палочкой, булавкой, головастиком. По своим размерам фаги относятся к средним по величине вирусам. Диаметр головки их составляет 60-90 мкм, длина отростка - 250 мкм, толщина - 10-25 мкм. Величина фагов довольно изменчива. Даже разные варианты одного и того же вида фага могут сильно различаться по своим размерам. Молекулярный вес фага 200 млн.
Частица фага является нуклеопротеидом и состоит из белка (50-60%) и ДНК (45-50%),которые фаги содержат небольшое количество липидов (1,5-2%). Белок образует оболочку фага, а ДНК находится во внутреннем пространстве головки фага. Белковая оболочка состоит из большого числа белковых частиц называемых субъединицами.
Физические и Химические свойства
Клетка бактерии-хозяина является средой для бактериофага, откуда он черпает вещества, необходимые для роста и размножения. Фаги более устойчивы к действию физических и химических факторов, чем неспороносные бактерии. В запаянных пробирках фаги могут сохраняться годами. Большинство фагов инактивируется при 65-75°С. Фаги очень чувствительны к действию кислот и устойчивы к действию антибиотиков.
Малые бактериофаги с икосаэдрической формой вириона содержат только белок и нуклеиновую кислоту типа РНК (Леб и Циндер, 1961; Купер и Циндер, 1962; Штраус и Синсхеймер, 1963) или ДНК (Патнем, 1963). У двух описанных нитевидных бактериофагов содержится белок и ДНК.
Крупные спермиеобразные бактериофаги, из которых наиболее изучены" бактериофаги 7 П -четной серии, поражающие Escherichia coli имеют сложный белковый состав и нуклеиновую кислоту типа ДНК. По структурным и функциональным особенностям белки бактериофага Т4 распределяются следующим образом:
1. Белковая оболочка головки.
2. Белок «чехла» отростка, обладающий сократительной функцией.
3. Белок проксимальной части отростка, обладающий ферментной логической активностью в отношении бактериальной оболочки.
4. Белок дистальной части отростка, служащий для прикрепления бактериофага к оболочке бактерии - хозяина.
5. Белок стержня отростка.
6.Внутренний белок с неизвестной функцией, находящийся в головке и связавший с системой ДНК.
Почти половина азота бактериофага Т2 приходится на белок, а другая половина - на
ДНК. Около 7% азота содержит кислотнорастворимый материал, химическая природа
которого не установлена. Почти весь фосфор (99%) входит в состав ДНК и только 1 %
его связан с кислотнорастворимой фракцией.
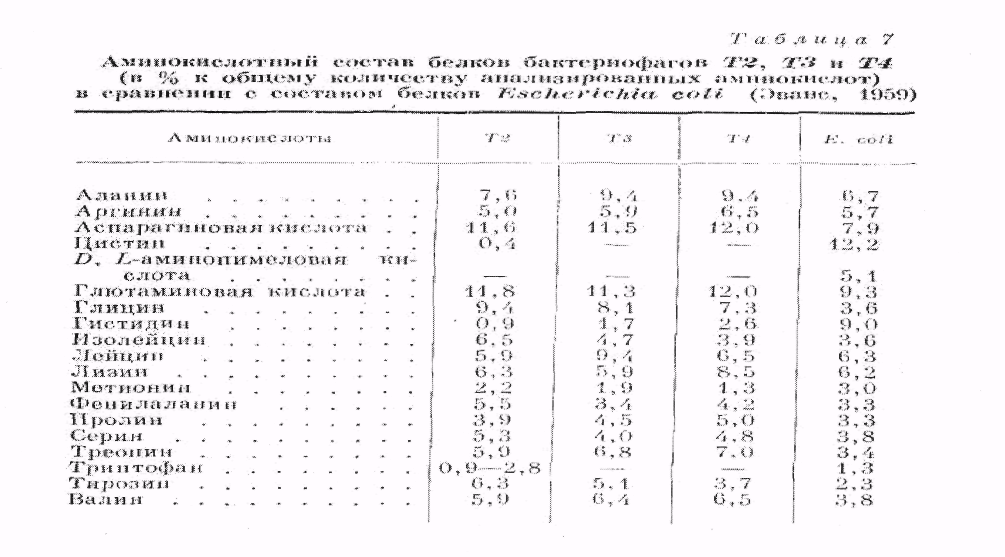
В табл. 7 представлен аминокислотный состав белка бактериофагов Т2, ТЗ - и Т4 и
бактерии-хозяина.
Разнообразие бактериофагов
Важным свойством фагов является их специфичность. Каждый вид фага специфичен к определенному виду микробов. Фаги, лизирующие актиномицеты, называются актинофагами, растворяющие грибы - микофагами, сине-зеленые организмы (цианобактерий) - цианофагами.
В зависимости от вида поражающих бактерий и вызываемые болезни или процессы фаги подразделяются на:
Лизогеннический бактериофаг
Литический бактериофаг
Вегетативный бактериофаг
Кишечный бактериофаг
Стрептококковый бактериофаг
Холерный бактериофаг
Чумной бактериофаг
Происхождение и природа Бактериофагов
Внутриклеточное развитие и явление лизогения
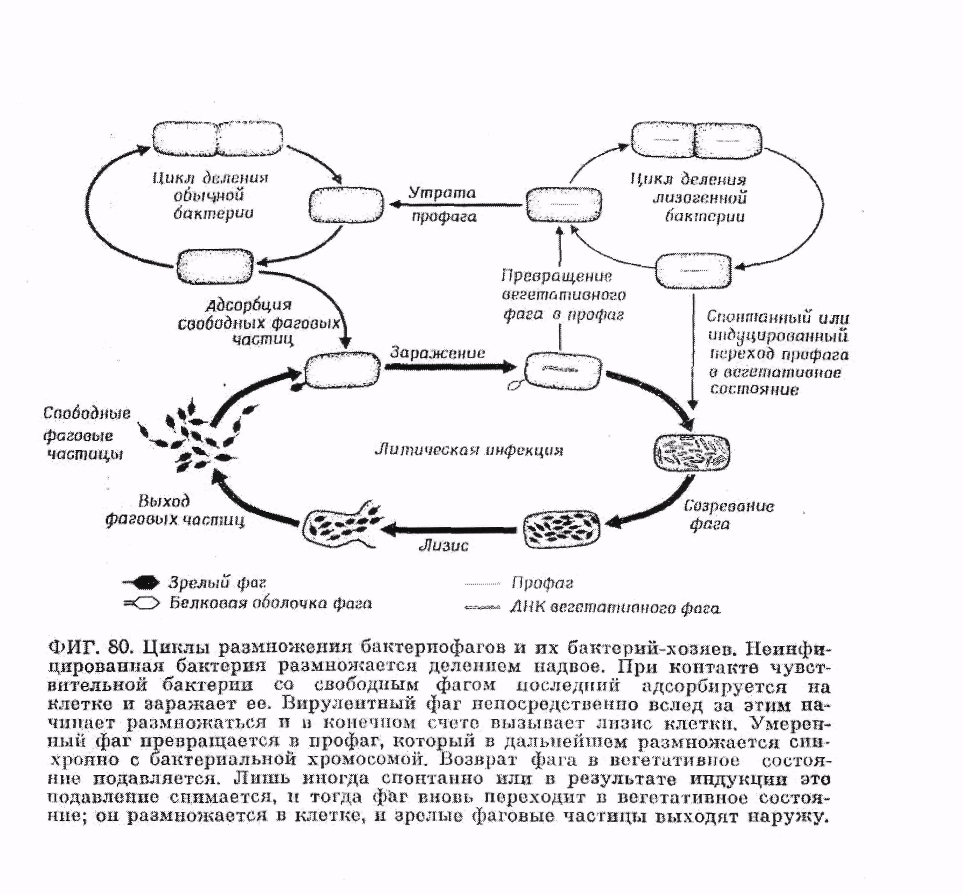
Описанные выше бактериофаги неизменно лизируют зараженные ими бактерии, и потому их называют вирулентными. Некоторые фаги, однако, заражают бактерий-хозяев, но не размножаются в них автономно и не вызывают лизиса. Такие фаги называются умеренными. Видимо, их размножение происходит синхронно с размножением бактерии. Лишь иногда, в одной из 10 2 ... 10 5 таких лизогеиных бактерий, фаг начинает спонтанно размножаться и клетка лизируется. Чтобы обнаружить выход инфекционного фага, в этом случае требуется - в качестве индикатора - другой бактериальный штамм, для которого этот фаг вирулентен. Если смешать лизогенные бактерии с избытком бактерий-индикаторов
и высеять их на агаризованную питательную среду, то будет наблюдаться рост колоний лизогенных бактерий. Время от времени некоторые клетки будут лизироваться и выходящие из них фаговые частицы будут заражать находящиеся по соседству чувствительные (индикаторные) бактерии. Это приведет к появлению бляшек в сплошном бактериальном газоне. Однако в середине каждой такой бляшки сохранится колония лизогенной бактерии (фиг. 79).
Размножение бактериофагов 1. условие размножения
Клетка бактерии-хозяина является средой для бактериофага, откуда он черпает вещества, необходимые для роста и размножения. Это, прежде всего относится к аминокислотам и компонентам нуклеиновых кислот. Если в питательной среде отсутствуют отдельные аминокислоты, без которых данный вид бактерии не проявляет роста, то и бактериофаг не размножается.
При благоприятных условиях размножения масса вновь образующихся корпускул бактериофага составляет 0,1 или даже более массы бактериальной клетки. Применение меченых изотопов позволило установить, что на построение тола бактериофага используются вещества как заранее синтезированные клеткой еще до со заражения, так и синтезированные ею уже в процессе инфекции. Например, фосфор ДНК бактериофага Т2 в количестве до 25% берется из соединений, ранее синтезированных клеткой, и на 75% используется из веществ, накопленных после заражения, в то время как белковый азот на 90% ассимилируется из соединений, образовавшихся после
заражения. В случае бактериофага Т7, до 80% фосфора используется из первоначальных запасов хозяина (Лабау, 1951). Имеются указания, что фосфор, входящий в состав бактериофага Т5, не связан с ДНК бактерии, поскольку он извлекается бактерией из среды всего лишь за 2 мин до заражения.
Приведенные данные показывают, что и белок, и нуклеиновая кислота бактериофага синтезируются из низкомолекулярных соединений, при внедрении бактериофага дыхание бактерии не изменяется. Однако при блокировке процессов, обеспечивающих энергетические ресурсы клетки, размножение бактериофага прекращается. Напротив, при некоторых воздействиях, препятствующих делению бактериальных клеток, но не прекращающих метаболические процессы, например, при действии пенициллина или ультрафиолетовой радиации, бактериофаг размножается беспрепятственно. Отсюда можно заключить, что между размножением бактерии-хозяина и бактериофага прямых коррелятивных связей не существует.
Репродукция бактериофага вызывает глубокие патологические изменения в метаболизме бактериальных клеток. У ряда патогенных и непатогенных микроорганизмов к результате заражения их бактериофагом снижается способность разлагать углеводы. В то же время наблюдается активирование комплекса восстановительных ферментов (Клейн и Шур-Шульц, 1947, 1948а, б). У кишечной палочки, зараженной бактериофагом, возрастает активность дегидраз (Клейн, 1954).
Лизис зараженных бактерии происходят, но окончании латентного периода, продолжительность которого различна у разных видов бактериофага. Лизис не связан с образованием инфекционного бактериофага, поскольку он наступает и в том случае, если под действием проф лавина развитие бактериофага нарушается, и вместо нормальных вирионов возникают дефективные неинфекционные частицы (Де Марс и др., 1953). По-видимому, биологической причиной лизиса являются процессы, связанные с размножением бактериофага и с переходом его в фазу покоя независимо от того, происходит ли этот переход нормально или абортивное. Во всяком случае, продолжительность латентного периода остается одинаковой при весьма больших колебаниях продолжительности генеративного цикла бактерии-хозяина, достигающих пятикратного размера из-за различных влияний внешней среды. 2. размножение
Процесс заражения бактериофагом бактериальной клетки начинается с адсорбции вирионов бактериофага на ее оболочке.
Бактериофаги на бактериальных клетках адсорбируются при всех градациях температуры от 0 до 37° С. Однако бактериофаг Т2 при низкой температуре исторгает генеративный материал не в клетку, а л окружающую среду и заражения бактерии
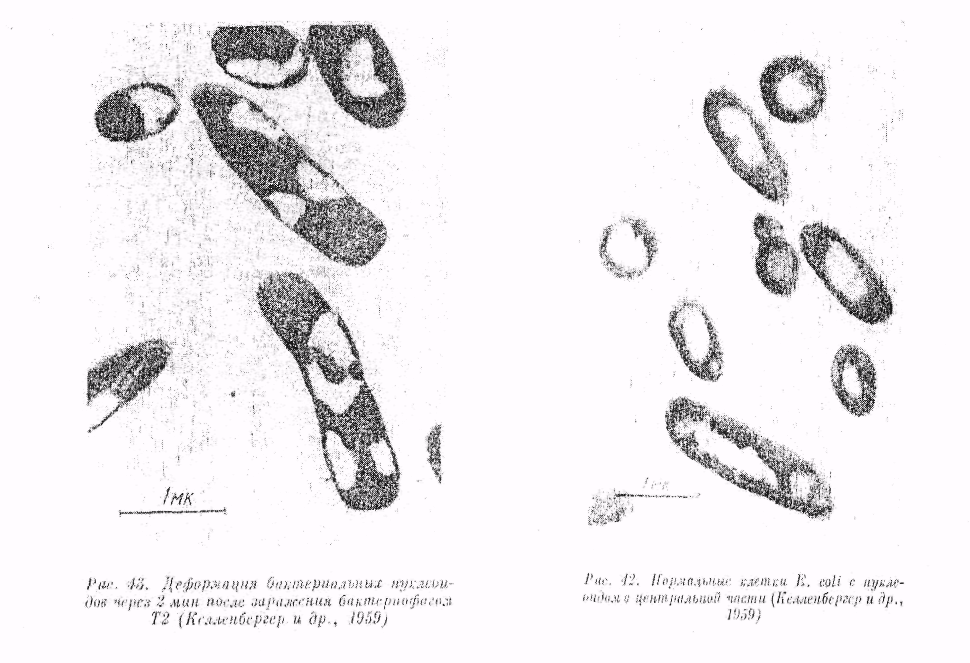
не происходит.
Размножение Вирулентного фага. Литический цикл
Размножение вируса в клетке-хозяине - весьма сложный процесс. Отдельные этапы этого процесса - от заражения клетки-хозяина до освобождения зрелых вирусных частиц, способных в свою очередь произвести заражение - довольно хорошо изучены с биохимической, генетической и морфологической стороны на примере фагов Т-серии (фаги Т2, Т4, ТО). Благоприятной предпосылкой для таких исследований явилось то обстоятельство, что в фаговой ДНК вместо цитозина содержится 5-оксиметшщитозин, а потому ее синтез легко проследить по появлению этого основания. Можно получить мутанты фага, у которых та или иная стадия процесса размножения блокирована или же протекает только в определенных условиях. Опыты с такими мутантами позволяют установить, как происходит в клетке-хозяине морфологическое развитие (морфопоэз) фага, т. е. в какой временной последовательности синтезируются и соединяются субъединицы фаговых частиц.
Подобно другим вирусам, фаги неподвижны. При смешивании суспензии свободных фагов с суспензией бактерий фаговые частицы в результате случайных столкновений с клетками прикрепляются к поверхности этих последних (адсорбция) и вводят в клетку свою ДНК (инъекция). После некоторого периода, на протяжении которого происходят процессы синтеза и созревания, клетки лизируются и новообразованные фаговые частицы выходят наружу.
Адсорбция. Не всякий фаг адсорбируется на всякой бактерии. Специфичность фага в отношении хозяина определяется специфичностью адсорбции. Последняя зависит от рецепторов, имеющихся в клеточной стенке; рецепторы для одних фагов
Внутриклеточное развитие фага. За адсорбцией следует инъекция, введение ДНК в клетку. У фага Т2 при этом базальная пластинка фиксируется на клетке, чехол отростка сокращается и ч полый стержень (благодаря этому сокращению) входит в клетку. Опыты с фагом, у которого нуклеиновая кислота и белок несли разную метку (соответственно Р и S), показали, что в клетку попадает только нуклеиновая кислота, а белковая оболочка остается снаружи. Если отделить эту оболочку от зараженной клетки, размножение фага не нарушится. Во время так называемого скрытого периода (эклипс), продолжающегося у Escherichia coli в среднем 25 мин, в искусственно разрушенных бактериальных клетках не удается обнаружить фага. Фаговая ДНК, прежде всего, вызывает полную перестройку обмена веществ инфицированной клетки (фиг. 77). Тотчас же после заражения прекращается синтез бактериальной ДНК. Через несколько минут прекращается также синтез бактериальной РНК и бактериального белка, хотя общее содержание белка продолжает непрерывно увеличиваться. Затем синтез ДНК возобновляется, причем с повышенной скоростью. Сначала Фаговая ДНК образуется за счет распавшейся бактериальной. Эту перестройку и последующее новообразование фаговой ДНК можно количественно проследить по увеличению содержания 5-оксиметил-цитозипа - основания, специфичного для ДНК некоторых Т-фагов. Необходимые для синтеза фаговой ДНК ферменты образуются вскоре после заражения. Это так называемые «ранние белки». К «поздним белкам» относятся белки оболочки фага и фаговый лизоцим, или эндолизин; «поздние белки» образуются лишь во второй половине скрытого периода.
Заключительный процесс - созревание - состоит в соединении фаговой ДНК с белком оболочки и образовании зрелых инфекционных фаговых частиц. Созревание Лизогенные бактерии иммунные к заражению теми фагами, которые присутствуют в них в виде профага. Обеспечиваемый профагами иммунитет основывается не на отсутствии адсорбции (как при устойчивости к вирулентным фагам), а на образовании
особого цитоплазматического ропрессорного вещества, препятствующего размножению легетатипного фага. Это же ропрессорное вещество препятствует возврату профага is вегетативное состояние и подавляет синтез фаговых белков. Возникновение лизогенного состояния связано; таким образом, с образованием репрессора.
Спонтанно, без воздействия извне, лизогенные бактерии лизируются редко. Однако целый ряд факторов (ультрафиолетовые лучи и другие мутагенные агенты) может индуцировать в каждой клетке развитие профага, ведущее к образованию и выделению инфекционного фага. Успех такой индукции зависит от генетической конституции профага, физиологического состояния хозяина и условий культивирования. Индукция явно основывается па устранении или инактивации имеющихся молекул репрессора. Существуют мутанты умеренных фагов, вызывающие в клетке образование термолабильного репрессора. В этом случае для того, чтобы индуцировать лизис бактерий, достаточно просто повысить температуру до 44° С. Агенты, под действием которых происходит индукция,
по-видимому, вызывают накопление в клетке какого-то индуктора, инактивирующего репрессор.
Умеренные фаги могут также переходить в вирулентное состояние в результате мутации. Мутанты бывают двух типов. Одни мутанты оказываются устойчивыми к репрессору фага (они, поэтому могут размножаться и в лизогенных клетках, иммунных к обычным гомологичным фагам); другие мутанты утратили саму способность вызывать в клетке синтез репрессора. Этим, однако, дело не исчерпывается; вирулентные мутанты умеренных фагов отличаются от обычных вирулентных фагов по целому ряду физиологических признаков.
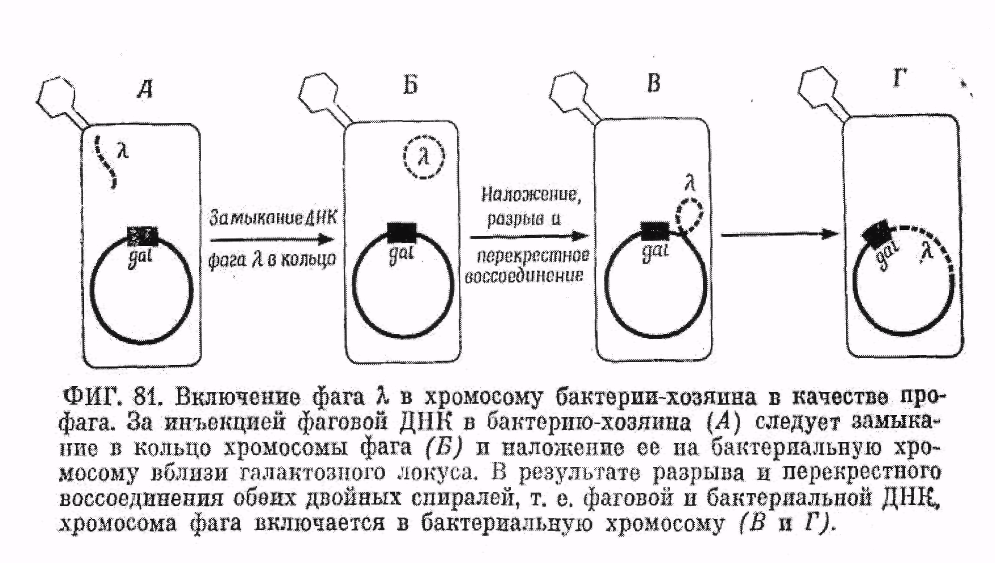
Интеграция и индукция фага К. Изучение фага X, лизогенного для Escherichia coli К 12, позволило установить, каким образом профаг связан с бактериальной хромосомой. Лизогенизация этим
фагом может служить примером жизненного цикла умеренного бактериофага. Длина хромосомы фага А, составляет всего около 2% длины бактериальной хромосомы. В свободных фаговых частицах ДНК присутствует в виде линейной двойной цепи. После инъекции в клетку-хозяина двойная цепь может замкнуться в кольцо.
В лизогенных клетках профаг прочно связан с хромосомой хозяина. При конъюгации клеток профаг вместе с хромосомой хозяина переносится из клетки-донора в клетку-реципиент. Генетические эксперименты показывают, что фаг X присоединен к хромосоме хозяина в совершенно определенном участке - между галактозным и биотиновым локусами. Соединение осуществляется па хромосоме или внутри нее. Сначала считалось, что ДНК профага только прикрепляется к хромосоме бактерии в этом участке. Однако в результате составления генетических карт фага, а также из опытов по рекомбинации стало ясно, что Фаговая ДНК при лизо^генизации не просто прикрепляется к бактериальной ДНК, а включается в нее. Такое включение профага {интеграция) происходит, очевидно, тем же путем, что и обмен ДНК при генетической рекомбинации, т. е. через разрыв и перекрестное воссоединение (фиг. 81). Поскольку Фаговая ДНК прикрепляется к бактериальной всегда в совершенно определенном месте, следует заключить, что у этих двух нуклеиновых кислот имеются гомологичные отрезки и что именно здесь происходит сначала наложение, а затем разрыв и воссоединение. Можно думать, что последовательности оснований фаговой и бактериальной ДНК в этих участках комплементарны.
В интегрированном состоянии Фаговая ДНК реплицируется вместе с бактериальной и подчиняется тем же регуляторным воздействиям, что и удвоение бактериальных хромосом. Информация, содержащаяся в фаговой ДНК, в это время выражения не находит.
Только в результате перехода профага в вегетативное состояние устанавливается автономия фаговой ДНК и начинается размножение фага. Этот обратный переход может происходить спонтанно или в результате индукции (например, при УФ-облучении). Отделение фаговой ДНК от бактериальной происходит, вероятно, путем, обратным включению, т. е. через образование петли ДНК и наложение гомологичных отрезков с последующим разрывом и новым замыканием кольца. Как только профаг в результате этого отделения перейдет в вегетативное состояние, он восстанавливает свою автономность; начиная с этого момента он перестает подчиняться репрессии и теперь уже размножается в бактериальной клетке как вирулентный фаг. Этот процесс приводит к лизису бактерий и высвобождению фага. Явление лизогении позволяет сделать вывод о существовании близкого родства между бактериями и бактериофагами. В основе его лежит, в конечном счете, довольно сильно выраженная гомологичность фаговой и бактериальной ДНК. Вирулентные фаги могут рассматриваться под этим углом зоения как продукт дальнейшего развития: они утратили гомологичность в отношении бактериальной ДНК и поэтому не могут более включаться в бактериальную хромосому; именно вследствие этого они и оказываются полностью автономными. На примере лизогенных бактерий видно, что многие вирусы могут быть самым тесным образом связаны с генетическим материалом клетки-хозяина и могут на протяжении многих поколений реплицироваться совместно с ним, ничем не обнаруживая своего присутствия.
Модификация фаговой ДНК
Фаги, как правило, проявляют специфичность в отношении хозяина. Определенный фаг поражает только один штамм бактерий или ограниченное число родственных штаммов, видов или родов; только в их клетках он способен размножаться. Такого рода специфичность обусловливается в первую очередь рецепторными свойствами поверхности бактериальной клетки. I Однако, помимо этого бактерии располагают и еще одной системой для распознавания фагов. Это распознавание зависит от фаговой ДНК. Речь идет о так называемой модификации фаговой ДНК, т. е. о незначительном ее изменении путем метилирования или гликозилирования пиримидиновых или пуриновых колец. Эти процессы происходят уже после образования фаговой ДНК в клетке-хозяине. Незначительное изменение ДНК никак не отражается на заключенной в ней генетической информации. Оно только позволяет клеткам «узнавать» ДНК. Это означает, что судьба такой ДНК в клетках разных бактериальных штаммов оказывается различной: в одних клетках эта ДНК разрушается, а в других - не разрушается и может реплицироваться. Разрушение фаговой ДНК нуклеазами зараженной клетки называют рестрикцией.
В качестве хорошо изученного примера можно привести фаг 12. При размножении этого фага в клетках Escherichia coli В конце латентного периода Фаговая ДНК глюкозируется. При этом более 65% остатков оксиметилцитозина, имеющихся в ДНК, присоединяют глюкозу. Если затем клетки Е. coli В заразить таким фагом, то фаг размножается в них и этот процесс всегда завершается лизисом. Но если фаг Т2 попадает в клетки дефектного мутанта Е. со/гВ, в которых глюкозилирование невозможно из-за недостатка УДФ-глюкозы (стр. 212), то при его размножении образуются частицы, несущие неглюкозилированную ДНК. Такие фаговые частицы (их обозначают через Т2 *) подчиняются рестрикции, т.е. они не могут размножаться в клетках Е. coli В. Во время инъекции в клетку их ДНК разрушается нуклеазой, локализованной в цито-плазматической мембране. Во всем остальном частицы Т2 * вполне интактны и способны к размножению. Они размножаются, например, в клетках Shigella , которые не содержат указанной нуклеазы Кроме того, клетки Shigella обладают глюкозилирующей системой; поэтому частицы Т2* претерпевают в них обратную модификацию, т. е. вновь превращаются в частицы Т2, способные размножаться в клетках Е. сои В. Модификацию претерпевают также ДНК фагов X и fd во время литического цикла в клетках Е. coli К. В ДНК этих фагов аминогруппы некоторых остатков аденина и цитозина метилируются. Фаговые частицы, содержащие такую метилированную ДНК, размножаются в клетках двух штаммов Е. coli , а именно Е. coli Ки£. coli В. Частицы же, содержащие неметилированную ДНК, в клетках штамма разрушаются. Имеются данные о том, что модификации подвергается не только Фаговая ДНК синтезирующаяся в бактериальных клетках, но также хромосомная и эписомная ДНК. Вполне возможно поэтому, что в основе известной несовместимости между партнерами при конъюгации и трансформации лежат механизмы, сходные с модификацией и рестрикцией.
Размножение вирусов
Строение вирусов
Зрелые вирусные частицы называются вирионами. Фактически они представляют собой геном, покрытый сверху белковой оболочкой. Эта оболочка- капсид . Она построена из белковых молекул, защищающих генетический материал вируса от воздействия нуклеаз - ферментов, разрушающих нуклеиновые кислоты.
У некоторых вирусов поверх капсида располагается суперкапсидная оболочка, также построенная из белка. Генетический материал представлен нуклеиновой кислотой. У одних вирусов это ДНК (так называемые ДНК-овые вирусы), у других - РНК (РНК-овые вирусы).
РНК-овые вирусы также называют ретровирусами, так как для синтеза вирусных белков в этом случае необходима обратная транскрипция, которая осуществляется ферментом - обратной транскриптазой (ревертазой) и представляет собой синтез ДНК на базе РНК.
В случае если это ретровирус, внутрь клетки-хозяина попадает его РНK. Она содержит гены, обеспечивающие обратную транскрипцию: на матрице РНК строится одноцепочечная молекула ДНК. Из свободных нуклеотидов достраивается комплементарная цепь, которая и встраивается в геном клетки-хозяина. С полученной ДНК информация переписывается на молекулу и-РНК, на матрице которой затем синтезируются белки ретровируса.
Взаимодействие вируса с живой клеткой 1. Адсорбция (прилипание) 2. Проникновение в клетку 3. Растворение белковой оболочки 4. Репликация (расщепление) нуклеиновой кислоты 5. Синтез белковой оболочки 6. Сборка вибриона 7. Выход вибриона из погибшей клетки 8.... [читать подробенее]
Впервые просветление взвеси палочек сибирской язвы наблюдал Н.Ф. Гамалея (1898), а пассируемый агент, который растворял шигеллы, выделил канадский ученый-бактериолог Ф.Д. Эррель (1916) и назвал его бактериофагом. Морфология бактериофага. Хорошо описанной является морфология... [читать подробенее]
Открытие вирусов Д.И.Ивановским в 1892г. положило начало развитию науки вирусологии. Более быстрому ее развитию способствовали: изобретение электронного микроскопа, разработка метода культивирования микроорганизмов в культурах клеток. Слово “вирус” в переводе с... [читать подробенее]
ВЕЗДЕ, ПОВСЮДУ Враг моего врага Люди знали о вирусах, или по крайней мере о вызываемых ими симптомах, все время, пока вирусы инфицировали людей. Ученые обнаружили существование вирусов в XIX веке, а к началу XX они узнали о них некоторые важные вещи. Выяснилось, что вирусы... [читать подробенее]
В 1915 году англичанин Фредерик Творт и канадец Феликс Д"Эрелль независимо друг от друга открыли бактериофаги, которые вызывают инфекции среди бактерий. Сама идея об инфекциях среди бактерий может показаться на первый взгляд странной, поскольку мы уверены, что инфекции... [читать подробенее]
Изменчивость микроорганизмов Различают генотипическую (наследуемую) изменчивость и фенотипическую (ненаследуемую, модификационную). Наследуемая изменчивость осуществляется в виде мутаций и рекомбинаций. Мутации- это перегруппировка генов, не связанная с...
>> Вирусы и бактериофаги
Вирусы и бактериофаги
1. Чем вирусы отличаются от других живых организмов?
2. Какие болезни могут вызывать вирусы?
Открытие вирусов.
Как уже говорилось, универсальной единицей жизни на Земле является . Однако на рубеже XIX и XX вв. было обнаружено, что существует целый ряд болезней растений, животных и бактерий, возбудители которых явно имеют неклеточную природу: они слишком малы и проходят через мельчайшие фильтры, которые задерживают даже самые маленькие клетки. Так были открыты вирусы.
Строение вирусов.
Размножение вирусов.
Обычно вирус связывается с поверхностью клетки-хозяина и проникает внутрь. При этом каждый вирус ищет именно «своего» хозяина, т. е. клетки строго определенного вида. Так, вирус - возбудитель гепатита, называемого иначе желтухой, проникает и размножается только в клетках печени, а вирус эпидемического паротита, в просторечии свинки, - только в клетках околоушных слюнных желез человека.
Проникнув внутрь клетки-хозяина, вирусная ДНК или РНК взаимодействует с хозяйским генетическим аппаратом таким образом, что клетка, сама того не желая, начинает синтезировать специфические белки, закодированные в вирусной нуклеиновой кислоте.
Последняя тоже реплицируется, и в цитоплазме клетки начинается сборка новых вирусных частиц. Пораженная вирусами клетка может буквально «лопнуть», и из нее выйдет большое число вирусных частиц, но иногда вирусы выделяются из клетки постепенно, по одному, и зараженная клетка живет долго.
При заражении вирусом иммунодефицита человека (ВИЧ) РНК вируса самовоспроизводится вместе с РНК клетки. При этом человек какое-то время остается здоровым . Но затем вирус активируется, и развивается смертельное заболевание - СПИД (синдром приобретенного иммунодефицита). Вирусы являются возбудителями большого количества заболеваний человека: оспы, кори, гриппа, краснухи, бешенства, энцефалита и др. Известен также целый ряд заболеваний растений, вызываемых вирусами, например мозаичная болезнь табака, томатов, огурцов или скручивание листьев картофеля. Всего описано около 500 видов вирусов, поражающих клетки позвоночных животных, и около 300 вирусов растений. Некоторые вирусы участвуют в злокачественном перерождении клеток и тем самым провоцируют онкологические заболевания.
Бактериофаги.
Особой группой вирусов являются бактериофаги, или просто фаги, которые заражают бактериальные клетки. Фаг укрепляется на поверхности бактерии при помощи специальных «ножек» и вводит в ее цитоплазму полый стержень, через который, как через иглу шприца, проталкивает внутрь клетки свою ДНК или РНК. Таким образом, генетический материал фага попадает внутрь бактериальной клетки, а капсид остается снаружи. В цитоплазме начинается репликация генетического материала фага, синтез его белков, построение капсида и сборка новых фагов. Уже через 10 мин после заражения в бактерии формируются новые фаги, а через полчаса бактериальная клетка рвзрушается, и из нее выходят около 200 заново сформированных вирусов- фагов, способных заражать другие бактериальные клетки. Некоторые фаги используются человеком для борьбы с болезнетворными бактериями, например с бактериями, вызывающими холеру, дизентирию, брюшной тиф.
Капсид. Бактериофаг.
1. Можно ли вирусы считать особой формой жизни?
2. Какое строение имеют вирусы? В чем их отличие от других живых организмов?
3. Как вирусы размножаются?
4. Какие вирусы называют бактериофагами?
5. Какие предположения можно сделать о происхождении вирусов?
Иногда при воспроизведении генома вируса в него попадает и часть генома хозяина (это связано с особым механизмом репликации вирусной ДНК или РНК). Тогда при заражении других клеток модифицированные вирусы принесут в них и гены предыдущей клетки-хозяина.
Таким образом, некоторые вирусы способны переносить гены от одних клеток к другим. Этим объясняется частое использование вирусов в генной инженерии.
Название вирус (от лат. virus - т. е. яд) было предложено голландским ботаником Мартином Бейеринком в 1895 г., изучавшим болезни растений, вызываемые вирусами.
Каменский А. А., Криксунов Е. В., Пасечник В. В. Биология 10 класс
Отправлено читателями с интернет-сайта
Похожие статьи




